Sejarah singkat tentang serapan atom pertama kali diamati oleh
Frounhofer,
yang pada saat itu menelaah garis-garis hitam pada spectrum matahari.
Sedangkan yang memanfaatkan prinsip serapan atom pada bidang analisis
adalah seorang Australia bernama
Alan Walsh di
tahun 1995. Sebelumnya ahli kimia banyak tergantung pada cara-cara
spektrofotometrik atau metode spektrografik. Beberapa cara ini dianggap
sulit dan memakan banyak waktu, kemudian kedua metode tersebut segera
diagantikan dengan Spektrometri Serapan Atom (SSA).
Spektrometri Serapan Atom (SSA) adalah suatu alat yang digunakan pada
metode analisis untuk penentuan unsur-unsur logam dan metalloid yang
pengukurannya berdasarkan penyerapan cahaya dengan panjang gelombang
tertentu oleh atom logam dalam keadaan bebas . Metode ini sangat tepat
untuk analisis zat pada konsentrasi rendah. Teknik ini mempunyai
beberapa kelebihan dibandingkan dengan metode spektroskopi emisi
konvensional. Memang selain dengan metode serapan atom, unsur-unsur
dengan energi eksitasi rendah dapat juga dianalisis dengan fotometri
nyala, akan tetapi fotometri nyala tidak cocok untuk unsur-unsur dengan
energy eksitasi tinggi. Fotometri nyala memiliki range ukur optimum pada
panjang gelombang 400-800 nm, sedangkan AAS memiliki range ukur optimum
pada panjang gelombang 200-300 nm (Skoog et al., 2000).Untuk analisis
kualitatif, metode fotometri nyala lebih disukai dari AAS, karena AAS
memerlukan lampu katoda spesifik (hallow cathode). Kemonokromatisan
dalam AAS merupakan syarat utama. Suatu perubahan temperature nyala akan
mengganggu proses eksitasi sehingga analisis dari fotometri nyala
berfilter. Dapat dikatakan bahwa metode fotometri nyala dan AAS
merupakan komplementer satu sama lainnya.
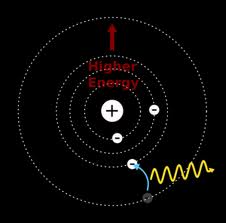
Metode AAS berprinsip pada absorbsi cahaya oleh atom, atom-atom
menyerap cahaya tersebut pada panjang gelombang tertentu, tergantung
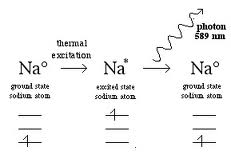
pada sifat unsurnya. Misalkan Natrium menyerap pada 589 nm, uranium pada
358,5 nm sedangkan kalium pada 766,5 nm. Cahaya pada gelombang ini
mempunyai cukup energy untuk mengubah tingkat energy elektronik suatu
atom. Dengan absorpsi energy, berarti memperoleh lebih banyak energy,
suatu atom pada keadaan dasar dinaikkan tingkat energinya ke tingkat
eksitasi. Tingkat-tingkat eksitasinya pun bermacam-macam. Misalnya unsur
Na dengan noor atom 11 mempunyai konfigurasi electron 1s
1 2s
2 2p
6 3s
1,
tingkat dasar untuk electron valensi 3s, artinya tidak memiliki
kelebihan energy. Elektronini dapat tereksitasi ketingkat 3p dengan
energy 2,2 eV ataupun ketingkat 4p dengan energy 3,6 eV, masing-masing
sesuai dengan panjang gelombang sebesar 589 nm dan 330 nm. Kita dapat
memilih diantara panjang gelombang ini yang menghasilkan garis spectrum
yang tajam dan dengan intensitas maksimum, yangdikenal dengan garis
resonansi. Garis-garis lain yang bukan garis resonansi dapat berupa
pita-pita lebar ataupun garis tidak berasal dari eksitasi tingkat dasar
yang disebabkan proses atomisasinya.
Contoh: prinsip dasar penyerapan atom Na

Apabila cahaya dengan panjang gelombang tertentu dilewatkan pada
suatu sel yang mengandung atom-atom bebas yang bersangkutan maka
sebagian cahaya tersebut akan diserap dan intensitas penyerapan akan
berbanding lurus dengan banyaknya atom bebas logam yang berada pada sel.
Hubungan antara absorbansi dengan konsentrasi diturunkan dari:
Hukum Lambert: bila suatu sumber sinar
monkromatik melewati medium transparan, maka intensitas sinar yang
diteruskan berkurang dengan bertambahnya ketebalan medium yang
mengabsorbsi.
Hukum Beer: Intensitas
sinar yang diteruskan berkurang secara eksponensial dengan bertambahnya
konsentrasi spesi yang menyerap sinar tersebut.
Dari kedua hukum tersebut diperoleh suatu persamaan:
A= ℮ b c dan A= abc serta persamaan A = – log T = log
Dimana:
P
O = intensitas sumber sinar
P = intensitas sinar yang diteruskan
℮ = absortivitas molar ( satuan c dalam Molar)
b = panjang medium / panjangnya jalan sinar
c = konsentrasi atom-atom yang menyerap sinar
A = absorbansi
T = Transmitan
a = absorbsivity ( satuan c dalam g/L atau ppm)
Dari persamaan di atas, dapat disimpulkan bahwa absorbansi cahaya
berbanding lurus dengan konsentrasi atom (Day & Underwood, 1989).
Prinsip Kerja Spektrometri Serapan Atom (SSA)
Metode AAS berprinsip pada absorpsi cahaya oleh atom. Atom-atom
menyerap cahaya tersebut pada panjang gelombang tertentu, tergantung
pada sifat unsurnya Spektrometri Serapan Atom (SSA) meliputi absorpsi
sinar oleh atom-atom netral unsur logam yang masih berada dalam keadaan
dasarnya (Ground state). Sinar yang diserap biasanya ialah sinar ultra
violet dan sinar tampak. Prinsip Spektrometri Serapan Atom (SSA) pada
dasarnya sama seperti absorpsi sinar oleh molekul atau ion senyawa dalam
larutan.
Hukum absorpsi sinar (Lambert-Beer) yang berlaku pada
spektrofotometer absorpsi sinar ultra violet, sinar tampak maupun infra
merah, juga berlaku pada Spektrometri Serapan Atom (SSA). Perbedaan
analisis Spektrometri Serapan Atom (SSA) dengan spektrofotometri molekul
adalah peralatan dan bentuk spectrum absorpsinya:
Setiap alat AAS terdiri atas tiga komponen yaitu:
- Unit atomisasi (atomisasi dengan nyala dan tanpa nyala)
- Sumber radiasi
- Sistem pengukur fotometri
Sistem Atomisasi dengan nyala
Setiap alat spektrometri atom akan mencakup dua komponen utama sistem introduksi sampeldan sumber (
source)
atomisasi. Untuk kebanyakan instrument sumber atomisasi ini adalah
nyata dan sampel diintroduksikan dalam bentuk larutan. Sampel masuk ke
nyala dalam bentuk aerosol. Aerosol biasanya dihasilkan oleh Nebulizer
(pengabut) yang dihubungkan ke nyala oleh ruang penyemprot (
chamber spray).
Ada banyak variasi nyala yang telah dipakai bertahun-tahun untuk
spektrometri atom. Namun demikian yang saat ini menonjol dan diapakai
secara luas untuk pengukuran analitik adalah udara asetilen dan nitrous
oksida-asetilen. Dengan kedua jenis nyala ini, kondisi analisis yang
sesuai untuk kebanyakan analit (unsur yang dianalisis) dapat sintetikan
dengan menggunakan metode-metode emisi, absorbsi dan juga fluoresensi.
Nyala udara asetilen
Biasanya menjadi pilihan untuk analisis menggunakan AAS. Temperature
nyalanya yang lebih rendah mendorong terbentuknya atom netral dan dengan
nyala yang kaya bahan bakar pembentukan oksida dari banyak unsur dapat
diminimalkan.
Nitrous oksida-asetilen
Dianjurkan dipakai untuk penentuan unsur-unsur yang mudah membentuk
oksida dan sulit terurai. Hal ini disebabkan temperature nyala yang
dihasilkan relatif tinggi. Unsur-unsur tersebut adalah: Al, B, Mo, Si,
Ti, V dan W.
Sistem Atomisasi tanpa Nyala (dengan Elektrotermal/tungku)
Sistem nyala api ini lebih dikenal dengan nama GFAAS. GFAAS dapat
mengatasi kelemahan dari sistem nyala seperti sensitivitas, jumlah
sampel dan penyiapan sampel.
Ada tiga tahap atomisasi dengan metode ini yaitu:
- Tahap pengeringan atau penguapan larutan
- Tahap pengabutan atau penghilangan senyawa-senyawa organic
- Tahap atomisasi
Unsur-unsur yang dapat dianalisis dengan menggunakan GFAAS adalah
sama dengan unsur-unsur yang dapat dianalisis dengan GFAAS tungsten: Hf,
Nd, Ho, La, Lu Os, Br, Re, Sc, Ta, U, W, Y dan Zr. Hal ini disebabkan
karena unsur tersebut dapat bereaksi dengan graphit.
Petunjuk praktis penggunaan GFAAS:
- Jangan menggunakan media klorida, lebih baik gunakan nitrat
- Sulfat dan fosfat bagus untuk pelarutsampel, biasanya setelah sampel ditempatkan dalam tungku.
- Gunakan cara adisi sehingga bila sampel ada interfensi dapat terjadi pada sampel dan standar.
- Untuk mengubah unsur metalik menjadi uap atau hasil disosiasi
diperlukan energy panas. Temperatur harus benar-benar terkendali dengan
sangat hati-hati agar proses atomisasinya sempurna. Ionisasi harus
dihindarkan dan ionisasi ini dapat terjadi apabila temperatur terlampau
tinggi. Bahan bakar dan oksidator dimasukkan dalam kamar pencamput
kemudian dilewatkan melalui baffle menuju ke pembakar. Hanya tetesan
kecil dapat melalui baffle. Tetapi kondisi ini jarang ditemukan, karena
terkadang nyala tersedot balik ke dalam kamar pencampur sehingga
menghasilkan ledakan. Untuk itu biasanya lebih disukai pembakar dengan
lubang yang sempit dan aliran gas pembakar serta oksidator dikendalikan
dengan seksama.
- Dengan gas asetilen dan oksidator udara bertekanan, temperature maksimum yang dapat tercapai adalah 1200
oC.
untuk temperatur tinggi biasanya digunakan N:O: = 2:1 karena banyaknya
interfensi dan efek nyala yang tersedot balik, nyala mulai kurang
digunakan, sebagai gantinya digunakan proses atomisasi tanpa nyala,
misalnya suatu perangkat pemanas listrik. Sampel sebanyak 1-2 ml
diletakkan pada batang grafit yang porosnya horizontal atau pada logam
tantalum yang berbentuk pipa. Pada tungku grafit temperatur dapat
dikendalikan secara elektris. Biasanya temperatur dinaikkan secara
bertahap, untuk menguapkan dan sekaligus mendisosiasi senyawa yang
dianalisis.
Metode tanpa nyala lebih disukai dari metode nyala. Bila ditinjau
dari sumber radiasi, metode tanpa nyala haruslah berasal dari sumber
yang kontinu. Disamping itu sistem dengan penguraian optis yang sempurna
diperlukan untuk memperoleh sumber sinar dengan garis absorpsi yang
semonokromatis mungkin. Seperangkat sumber yang dapat memberikan garis
emisi yang tajam dari suatu unsur spesifik tertentu dikenal sebagai
lampu pijar
Hollow cathode. Lampu ini memiliki dua elektroda,
satu diantaranya berbentuk silinder dan terbuat dari unsur yang sama
dengan unsur yang dianalisis. Lampuini diisi dengan gas mulia bertekanan
rendah, dengan pemberian tegangan pada arus tertentu, logam mulai
memijar dan atom-atom logam katodanya akan teruapkan dengan pemercikkan.
Atom akan tereksitasi kemudian mengemisikan radiasi pada panjang
gelombang tertentu.
Instrumen dan Alat

( gambar: perangkat AAS)
Untuk menganalisis sampel, sampel tersebut harus diatomisasi. Sampel
kemudian harus diterangi oleh cahaya. Cahaya yang ditransmisikan
kemudian diukur oleh detector tertentu.
Sebuah sampel cairan biasanya berubah menjadi gas atom melalui tiga langkah:
- Desolvation (pengeringan) – larutan pelarut menguap, dan sampel kering tetap
- Penguapan – sampel padat berubah menjadi gas
- Atomisasi – senyawa berbentuk gas berubah menjadi atom bebas.
Sumber radiasi yang dipilih memiliki lebar spectrum sempit
dibandingkan dengan transisi atom. Lampu katoda Hollow adalah sumber
radiasi yang paling umum dalam spekstroskopi serapan atom. Lampu katoda
hollow berisi gas argon atau neon, silinder katoda logam mengandung
logam untuk mengeksitasi sampel. Ketika tegangan yang diberikan pada
lampu meningkat, maka ion gas mendapatkan energy yang cukup untuk
mengeluarkan atom logam dari katoda. Atom yang tereksitasi akan kembali
ke keadaan dasar dan mengemisikan cahaya sesuai dengan frekuensi
karakteristik logam.
Bagian-Bagian pada AAS
Bentuk rangkaian alat AAS
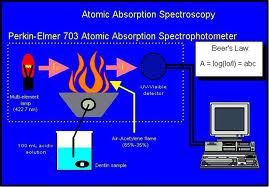

- Lampu Katoda
Lampu katoda merupakan sumber cahaya pada AAS. Lampu katoda memiliki
masa pakai atau umur pemakaian selama 1000 jam. Lampu katoda pada setiap
unsur yang akan diuji berbeda-beda tergantung unsur yang akan diuji,
seperti lampu katoda Cu, hanya bisa digunakan untuk pengukuran unsur Cu.
Lampu katoda terbagi menjadi dua macam, yaitu :
Lampu Katoda Monologam : Digunakan untuk mengukur 1 unsur
Lampu Katoda Multilogam : Digunakan untuk pengukuran beberapa logam sekaligus, hanya saja harganya lebih mahal.
Soket pada bagian lampu katoda yang hitam, yang lebih menonjol
digunakan untuk memudahkan pemasangan lampu katoda pada saat lampu
dimasukkan ke dalam soket pada AAS. Bagian yang hitam ini merupakan
bagian yang paling menonjol dari ke-empat besi lainnya.
Lampu katoda berfungsi sebagai sumber cahaya untuk memberikan energi
sehingga unsur logam yang akan diuji, akan mudah tereksitasi. Selotip
ditambahkan, agar tidak ada ruang kosong untuk keluar masuknya gas dari
luar dan keluarnya gas dari dalam, karena bila ada gas yang keluar dari
dalam dapat menyebabkan keracunan pada lingkungan sekitar.
Gambar hollow chatode



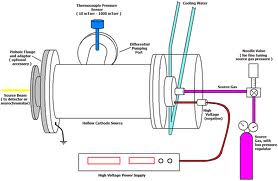
Cara pemeliharaan lampu katoda ialah bila setelah selesai digunakan,
maka lampu dilepas dari soket pada main unit AAS, dan lampu diletakkan
pada tempat busanya di dalam kotaknya lagi, dan dus penyimpanan ditutup
kembali. Sebaiknya setelah selesai penggunaan, lamanya waktu pemakaian
dicatat.
- Tabung Gas
Tabung gas pada AAS yang digunakan merupakan tabung gas yang berisi
gas asetilen. Gas asetilen pada AAS memiliki kisaran suhu ± 20.000K, dan
ada juga tabung gas yang berisi gas N
2O yang lebih panas
dari gas asetilen, dengan kisaran suhu ± 30.000K. Regulator pada tabung
gas asetilen berfungsi untuk pengaturan banyaknya gas yang akan
dikeluarkan, dan gas yang berada di dalam tabung. Spedometer pada bagian
kanan regulator merupakan pengatur tekanan yang berada di dalam tabung.
Pengujian untuk pendeteksian bocor atau tidaknya tabung gas tersebut,
yaitu dengan mendekatkan telinga ke dekat regulator gas dan diberi
sedikit air, untuk pengecekkan. Bila terdengar suara atau udara, maka
menendakan bahwa tabung gas bocor, dan ada gas yang keluar. Hal lainnya
yang bisa dilakukan yaitu dengan memberikan sedikit air sabun pada
bagian atas regulator dan dilihat apakah ada gelembung udara yang
terbentuk. Bila ada, maka tabung gas tersebut positif bocor. Sebaiknya
pengecekkan kebocoran, jangan menggunakan minyak, karena minyak akan
dapat menyebabkan saluran gas tersumbat. Gas didalam tabung dapat keluar
karena disebabkan di dalam tabung pada bagian dasar tabung berisi
aseton yang dapat membuat gas akan mudah keluar, selain gas juga
memiliki tekanan.
- Ducting
Ducting merupakan bagian cerobong asap untuk menyedot asap atau sisa
pembakaran pada AAS, yang langsung dihubungkan pada cerobong asap bagian
luar pada atap bangunan, agar asap yang dihasilkan oleh AAS, tidak
berbahaya bagi lingkungan sekitar. Asap yang dihasilkan dari pembakaran
pada AAS, diolah sedemikian rupa di dalam ducting, agar polusi yang
dihasilkan tidak berbahaya.
Cara pemeliharaan ducting, yaitu dengan menutup bagian ducting secara
horizontal, agar bagian atas dapat tertutup rapat, sehingga tidak akan
ada serangga atau binatang lainnya yang dapat masuk ke dalam ducting.
Karena bila ada serangga atau binatang lainnya yang masuk ke dalam
ducting , maka dapat menyebabkan ducting tersumbat.
Penggunaan ducting yaitu, menekan bagian kecil pada ducting kearah
miring, karena bila lurus secara horizontal, menandakan ducting
tertutup. Ducting berfungsi untuk menghisap hasil pembakaran yang
terjadi pada AAS, dan mengeluarkannya melalui cerobong asap yang
terhubung dengan ducting.
- Kompresor
Kompresor merupakan alat yang terpisah dengan main unit, karena alat
ini berfungsi untuk mensuplai kebutuhan udara yang akan digunakan oleh
AAS, pada waktu pembakaran atom. Kompresor memiliki 3 tombol pengatur
tekanan, dimana pada bagian yang kotak hitam merupakan tombol ON-OFF,
spedo pada bagian tengah merupakan besar kecilnya udara yang akan
dikeluarkan, atau berfungsi sebagai pengatur tekanan, sedangkan tombol
yang kanan merupakantombol pengaturan untuk mengatur banyak/sedikitnya
udara yang akan disemprotkan ke burner. Bagian pada belakang kompresor
digunakan sebagai tempat penyimpanan udara setelah usai penggunaan AAS.
Alat ini berfungsi untuk menyaring udara dari luar, agar
bersih.posisi ke kanan, merupakan posisi terbuka, dan posisi ke kiri
merupakan posisi tertutup. Uap air yang dikeluarkan, akan memercik
kencang dan dapat mengakibatkan lantai sekitar menjadi basah, oleh
karena itu sebaiknya pada saat menekan ke kanan bagian ini, sebaiknya
ditampung dengan lap, agar lantai tidak menjadi basah dan uap air akan
terserap ke lap.
- Burner
Burner merupakan bagian paling terpenting di dalam main unit, karena
burner berfungsi sebagai tempat pancampuran gas asetilen, dan aquabides,
agar tercampur merata, dan dapat terbakar pada pemantik api secara baik
dan merata. Lobang yang berada pada burner, merupakan lobang pemantik
api, dimana pada lobang inilah awal dari proses pengatomisasian nyala
api.
Perawatan burner yaitu setelah selesai pengukuran dilakukan, selang
aspirator dimasukkan ke dalam botol yang berisi aquabides selama ±15
menit, hal ini merupakan proses pencucian pada aspirator dan burner
setelah selesai pemakaian. Selang aspirator digunakan untuk menghisap
atau menyedot larutan sampel dan standar yang akan diuji. Selang
aspirator berada pada bagian selang yang berwarna oranye di bagian kanan
burner. Sedangkan selang yang kiri, merupakan selang untuk mengalirkan
gas asetilen. Logam yang akan diuji merupakan logam yang berupa larutan
dan harus dilarutkan terlebih dahulu dengan menggunakan larutan asam
nitrat pekat. Logam yang berada di dalam larutan, akan mengalami
eksitasi dari energi rendah ke energi tinggi.
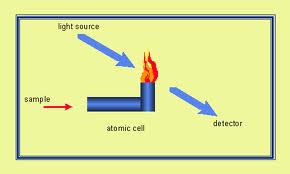

( Gambar : burner pada AAS)
Nilai eksitasi dari setiap logam memiliki nilai yang berbeda-beda.
Warna api yang dihasilkan berbeda-beda bergantung pada tingkat
konsentrasi logam yang diukur. Bila warna api merah, maka menandakan
bahwa terlalu banyaknya gas. Dan warna api paling biru, merupakan warna
api yang paling baik, dan paling panas.
- Buangan pada AAS
Buangan pada AAS disimpan di dalam drigen dan diletakkan terpisah
pada AAS. Buangan dihubungkan dengan selang buangan yang dibuat
melingkar sedemikian rupa, agar sisa buangan sebelumnya tidak naik lagi
ke atas, karena bila hal ini terjadi dapat mematikan proses
pengatomisasian nyala api pada saat pengukuran sampel, sehingga kurva
yang dihasilkan akan terlihat buruk. Tempat wadah buangan (drigen)
ditempatkan pada papan yang juga dilengkapi dengan lampu indicator. Bila
lampu indicator menyala, menandakan bahwa alat AAS atau api pada proses
pengatomisasian menyala, dan sedang berlangsungnya proses
pengatomisasian nyala api. Selain itu, papan tersebut juga berfungsi
agar tempat atau wadah buangan tidak tersenggol kaki. Bila buangan sudah
penuh, isi di dalam wadah jangan dibuat kosong, tetapi disisakan
sedikit, agar tidak kering.
- Monokromator
Berfungsi mengisolasi salah satu garis resonansi atau radiasi dari
sekian banyak spectrum yang dahasilkan oleh lampu piar hollow cathode
atau untuk merubah sinar polikromatis menjadi sinar monokromatis sesuai
yang dibutuhkan oleh pengukuran.
Macam-macam monokromator yaitu prisma, kaca untuk daerah sinar
tampak, kuarsa untuk daerah UV, rock salt (kristal garam) untuk daerah
IR dan kisi difraksi.
- Detector
Dikenal dua macam detector, yaitu detector foton dan detector panas.
Detector panas biasa dipakai untuk mengukur radiasi inframerah termasuk
thermocouple dan bolometer. Detector berfungsi untuk mengukur intensitas
radiasi yang diteruskan dan telah diubah menjadi energy listrik oleh
fotomultiplier. Hasil pengukuran detector dilakukan penguatan dan
dicatat oleh alat pencatat yang berupa printer dan pengamat angka.
Ada dua macam deterktor sebagai berikut:
-
Detector Cahaya atau Detector Foton
Detector foton bekerja berdasarkan efek fotolistrik, dalam halini
setiap foton akan membebaskan elektron (satu foton satu electron) dari
bahan yang sensitif terhadap cahaya. Bahan foton dapat berupa Si/Ga,
Ga/As, Cs/Na.
-
Detector Infra Merah dan Detector Panas
Detector infra merah yang lazim adalah termokopel. Efek termolistrik
akan timbul jika dua logam yang memiliki temperatur berbeda disambung
jadi satu.
Bentuk spectra AAS
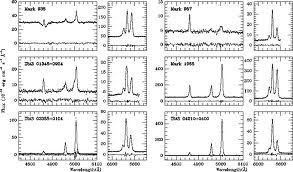 Cara kerja spektrofotometer serapan atom
Cara kerja spektrofotometer serapan atom
- Pertama-tama gas di buka terlebih dahulu, kemudian kompresor, lalu ducting, main unit, dan komputer secara berurutan.
- Di buka program SAA (Spectrum Analyse Specialist), kemudian
muncul perintah ”apakah ingin mengganti lampu katoda, jika ingin
mengganti klik Yes dan jika tidak No.
- Dipilih yes untuk masuk ke menu individual command, dimasukkan
nomor lampu katoda yang dipasang ke dalam kotak dialog, kemudian
diklik setup, kemudian soket lampu katoda akan berputar menuju
posisi paling atas supaya lampu katoda yang baru dapat diganti atau
ditambahkan dengan mudah.
- Dipilih No jika tidak ingin mengganti lampu katoda yang baru.
- Pada program SAS 3.0, dipilih menu select element and working
mode.Dipilih unsur yang akan dianalisis dengan mengklik langsung
pada symbol unsur yang diinginkan
- Jika telah selesai klik ok, kemudian muncul tampilan condition
settings. Diatur parameter yang dianalisis dengan mensetting fuel
flow :1,2 ; measurement; concentration ; number of sample: 2 ; unit
concentration : ppm ; number of standard : 3 ; standard list : 1
ppm, 3 ppm, 9 ppm.
- Diklik ok and setup, ditunggu hingga selesai warming up.
- Diklik icon bergambar burner/ pembakar, setelah pembakar dan lampu menyala alat siap digunakan untuk mengukur logam.
- Pada menu measurements pilih measure sample.
- Dimasukkan blanko, didiamkan hingga garis lurus terbentuk, kemudian dipindahkan ke standar 1 ppm hingga data keluar.
- Dimasukkan blanko untuk meluruskan kurva, diukur dengan tahapan yang sama untuk standar 3 ppm dan 9 ppm.
- Jika data kurang baik akan ada perintah untuk pengukuran ulang,
dilakukan pengukuran blanko, hingga kurva yang dihasilkan turun
dan lurus.
- Dimasukkan ke sampel 1 hingga kurva naik dan belok baru dilakukan pengukuran.
- Dimasukkan blanko kembali dan dilakukan pengukuran sampel ke 2.
- Setelah pengukuran selesai, data dapat diperoleh dengan
mengklikicon print atau pada baris menu dengan mengklik file lalu
print.
- Apabila pengukuran telah selesai, aspirasikan air deionisasi
untuk membilas burner selama 10 menit, api dan lampu burner
dimatikan, program pada komputer dimatikan, lalu main unit AAS,
kemudian kompresor, setelah itu ducting dan terakhir gas.
Metode Analisis
Adatiga teknik yang biasa dipakai dalam analisis secara spektrometri. Ketiga teknik tersebut adalah:
- 1. Metode Standar Tunggal
Metode ini sangat praktis karena hanya menggunakan satu larutan
standar yang telah diketahui konsentrasinya (Cstd). Selanjutnya absorbsi
larutan standar (Asta) dan absorbsi larutan sampel (Asmp) diukur dengan
spektrometri. Dari hukum Beer diperoleh:
Sehingga,
Astd/Cstd = Csmp/Asmp -> Csmp = (Asmp/Astd) x Cstd
Dengan mengukur absorbansi larutan sampel dan standar, konsentrasi larutan sampel dapat dihitung.
- 2. Metode kurva kalibrasi
Dalam metode ini dibuat suatu seri larutan standar dengan berbagai
konsentrasi dan absorbansi dari larutan tersebut diukur dengan AAS.
Langkah selanjutnya adalah membuat grafik antara konsentrasi(C) dengan
absorbansi (A) yang merupakan garis lurus yang melewati titik nol dengan
slobe = atau = a.b. konsentrasi larutan sampel dapat dicari setelah
absorbansi larutan sampel diukur dan diintrapolasi ke dalam kurva
kalibrasi atau dimasukkan ke dalam persamaan garis lurus yang diperoleh
dengan menggunakan program regresi linewar pada kurvakalibrasi.
- 3. Metode adisi standar
Metode ini dipakai secara luas karena mampu meminimalkan kesalahan
yang disebabkan oleh perbedaan kondisi lingkungan (matriks) sampel dan
standar. Dalam metode ini dua atau lebih sejumlah volume tertentu dari
sampel dipindahkan ke dalam labu takar. Satu larutan diencerkan sampai
volume tertentu kemudiaan larutan yang lain sebelum diukur absorbansinya
ditambah terlebih dahulu dengan sejumlah larutan standar tertentu dan
diencerkan seperti pada larutan yang pertama.
Menurut hukum Beer akan berlaku hal-hal berikut:
Ax = k.Ck AT = k(Cs+Cx)
Dimana,
Cx = konsentrasi zat sampel
Cs = konsentrasi zat standar yang ditambahkan ke larutan sampel
Ax = absorbansi zat sampel (tanpa penambahan zat standar)
AT = absorbansi zat sampel + zat standar
Jika kedua rumus digabung maka akan diperoleh Cx = Cs + {Ax/(AT-Ax)}
Konsentrasi zat dalam sampel (Cx) dapat dihitung dengan mengukur Ax
dan AT dengan spektrometri. Jika dibuat suatu seri penambahan zat
standar dapat pula dibuat grafik antara AT lawan Cs garis lurus yang
diperoleh dari ekstrapolasi ke AT = 0, sehingga diperoleh:
Cx = Cs x {Ax/(0-Ax)} ; Cx = Cs x (Ax/-Ax)
Cx = Cs x (-1) atau Cx = -Cs
Salah satu penggunaan dari alat spektrofotometri serapan atom adalah
untuk metode pengambilan sampel dan analisis kandungan logam Pb di
udara. Secara umum pertikulat yang terdapat diudara adalah sebuah sistem
fase multi kompleks padatan dan partikel-partikel cair dengan tekanan
uap rendah dengan ukuran partikel antara 0,01 – 100 μm.
Keuntungan danKelemahan Metode AAS
Keuntungan metode AAS dibandingkan dengan spektrofotometer biasa
yaitu spesifik, batas deteksi yang rendah dari larutan yang sama bisa
mengukur unsur-unsur yang berlainan, pengukurannya langsung terhadap
contoh, output dapat langsung dibaca, cukup ekonomis, dapat
diaplikasikan pada banyak jenis unsur, batas kadar penentuan luas (dari
ppm sampai %).
Sedangkan kelemahannya yaitu pengaruh kimia dimana AAS tidak mampu
menguraikan zat menjadi atom misalnya pengaruh fosfat terhadap Ca,
pengaruh ionisasi yaitu bila atom tereksitasi (tidak hanya disosiasi)
sehingga menimbulkan emisi pada panjang gelombang yang sama, serta
pengaruh matriks misalnya pelarut.
Gangguan-gangguan dalam metode AAS
- Ganguan kimia
Gangguan kimia terjadi apabila unsur yang dianailsis mengalami reaksi
kimia dengan anion atau kation tertentu dengan senyawa yang refraktori,
sehingga tidak semua analiti dapat teratomisasi. Untuk mengatasi
gangguan ini dapat dilakukan dengan dua cara yaitu: 1) penggunaan suhu
nyala yang lebih tinggi, 2) penambahan zat kimia lain yang
dapatmelepaskan kation atau anion pengganggu dari ikatannya dengan
analit. Zat kimia lai yang ditambahkan disebut zat pembebas (
Releasing Agent) atau zat pelindung (
Protective Agent).
- Gangguang Matrik
Gangguan ini terjadi apabila sampel mengandung banyak garam atau
asam, atau bila pelarut yang digunakan tidak menggunakan pelarut zat
standar, atau bila suhu nyala untuk larutan sampel dan standar berbeda.
Gangguan ini dalam analisis kualitatif tidak terlalu bermasalah, tetapi
sangat mengganggu dalam analisis kuantitatif. Untuk mengatasi gangguan
ini dalam analisis kuantitatif dapat digunakan cara analisis penambahan
standar (Standar Adisi).
- Gangguan Ionisasi
Gangguan ionisasi terjadi bila suhu nyala api cukup tinggi sehingga
mampu melepaskan electron dari atom netral dan membentuk ion positif.
Pembentukan ion ini mengurangi jumlah atom netral, sehingga isyarat
absorpsi akan berkurang juga. Untuk mengatasi masalah ini dapat
dilakukan dengan penambahan larutan unsur yang mudah diionkan atau atom
yang lebih elektropositif dari atom yang dianalisis, misalnya Cs, Rb, K
dan Na. penambahan ini dapat mencapai 100-2000 ppm.
- Absorpsi Latar Belakang (Back Ground)
Absorbsi Latar Belakang (Back Ground) merupakan istilah yang
digunakan untuk menunjukkan adanya berbagai pengaruh, yaitu dari
absorpsi oleh nyala api, absorpsi molecular, dan penghamburan cahaya.
Analisis Kuantitatif
- Penyiapan sampel
Penyiapan sampel sebelum pengukuran tergantung dari jenis unsur yang ditetapkan, jenis substrat dari sampel dan cara atomisasi.
Pada kebanyakan sampel hal ini biasanya tidak dilakukan,bila
atomisasi dilakukan menggunakan batang grafik secara elektrotermal
karena pembawa (matriks) dari sampel dihilangkan melalui proses
pengarangan (ashing) sebelumatomisasi.Pada atomisasi dengan nyala,
kebanyakan sampel cair dapat disemprotkan langsung ke dalam nyala
setelah diencerkan dengan pelarut yang cocok..Sampel padat
biasanya dilarutkan dalam asam tetaou adakalanya didahului dengan
leburan alkali.
- Analisa kuantitatif
Pada analisis kuantitatif ini kita harus mengetahui beberapa hal
perlu diperhatikan sebelum menganalisa.Selain itu kita harus mengetahui
kelebihan dan kekurangan pada AAS.
Beberapa hal yang perlu diperhatikan sebelum menganalisa:
- Larutan sampel diusahakan seencer mungkin (konsentrasi ppm atau ppb).
- Kadar unsur yang dianalisistidaklebihdari 5% dalampelarut yang sesuai.
- Hindari pemakaian pelarut aromatic atau halogenida. Pelarut
organic yang umum digunakan adalah keton, ester dan etilasetat.
- Pelarut yang digunakan adalah pelarut untuk analisis (p.a)
Langkah analisis kuantitatif:
- PembuatanLarutanStokdan LarutanStandar
- Pembuatan Kurva Baku
Persamaan garis lurus : Y = a + bx dimana:
a = intersep
b = slope
x = konsentrasi
Y = absorbansi
Penentuan kadar sampel dapat dilakukan dengan memplotkan data
absorbansi terhadap konsentrasi atau dengan cara mensubstitusikan
absorbansi kedalam persamaangaris lurus
( sumber: digabungkan dari berbagai sumber)